«Фармаксі»: як в Україні досліджують ліки на людях і чому вам не треба боятися вакцин від COVID-19
Вакцина від коронавірусу CoviShield показала ефективність 70,4%, але українці їй не довіряють. За результатами опитування Центру Разумкова, 51,5% українців не збираються робити щеплення цією вакциною, 45,2% з них вважають CoviShield недостатньо безпечною.
Серед тих, хто досліджує ефективність вакцин і ліків в Україні, – компанія «Фармаксі». Вона на ринку вісім років, на замовлення українських і зарубіжних фармкомпаній вивчала приблизно 40 препаратів, у тому числі ліки від раку та СНІДу.
У партнерському проєкті з «Фармаксі» MC.today розповідає, як проходять дослідження препаратів, що вони дають українцям і чому вакцинам від коронавірусу, які використовують в Україні, можна довіряти.
Що таке клінічні дослідження
Перед тим як будь-які вакцини або ліки починають використовувати люди, проводять їх клінічні дослідження. Це науковий метод, за допомогою якого вивчають, наскільки препарати є безпечними й ефективними.
Мало хто знає, що важливість клінічних досліджень перевершує багато відкриттів останніх 50 років. Цей науковий метод буквально рятує життя.

Юрій Лебідь, засновник «Фармаксі»
Аспірин застосовується для профілактики інфаркту, тромболітичні препарати можуть розчинити тромб і запобігти інсульту, антибіотики допомагають вилікувати пневмонію, від якої раніше вмирали. Це було б неможливо без клінічних досліджень.
Ліки та вакцини, які успішно пройшли клінічні випробування, допомагають позбутися небезпечних інфекцій і хвороб. Наприклад, завдяки глобальній вакцинації вдалося перемогти натуральну віспу – причину жахливих епідемій в минулому.
У препаратів можуть бути побічні ефекти, про які попереджають в інструкції. Цю інформацію виробник теж отримує під час клінічних досліджень.
«Дослідження можна провести і за $50 тис., і за $1 млн. Усе залежить від складності і тривалості лікування хвороби, числа лікарів і пацієнтів, яких залучають до тестування, умов зберігання препарату й інших чинників, – розповідає експерт. – Наш найбільший чек – $700 тис.».
Як фармкомпанії готуються до досліджень
До старту тестування на людях безпеку препаратів перевіряють у лабораторіях і на тваринах: щурах, мишах, кроликах. «Справа в тому, що організм тварин-ссавців працює в основному так само, як і людський організм. Фізіологія людини і щура схожа, – пояснює Юрій. – Якщо ліки є нетоксичними для тварини, вони навряд чи викличуть значні побічні ефекти в людини. Зрозуміло, що відмінності є і побічні ефекти можуть виявитися. Але щоб це з’ясувати, і проводять клінічні дослідження на пацієнтах». Тільки переконавшись, що ліки є нетоксичними і не викликають важких побічних ефектів у тварин, фармакологічна компанія переходить до клінічних випробувань.
Щоб отримати дозвіл на них, виробник збирає безліч документів, де описана технологія виробництва, механізм дії препарату та багато іншого. Їх подають до Державного експертного центру МОЗ України або аналогічного відомства в іншій державі.
До «Фармаксі» кілька разів зверталися із проханням провести клінічне дослідження препарату, за яким не зібрали всю необхідну документацію. У цих випадках замовникам відмовляли: з таким обсягом документів немає сенсу подавати заявку в Експертний центр.
«Поки фармакологічна компанія не надасть переконливі дані, що препарат є безпечним для людей, клінічні дослідження не схвалять у жодній країні світу, у тому числі в Україні», – підкреслює співзасновник «Фармаксі».
Серед документів, які подають в експертний центр, – протокол клінічних досліджень. У ньому вказують, скільки пацієнтів потрібно залучити, які параметри їхнього здоров’я виміряти, скільки повинно тривати лікування тощо. Документ готує сама фармакологічна компанія або підрядники на кшталт «Фармаксі».
У команді Юрія Лебідя протоколи складає відділ клінічних операцій, у якому працюють люди з медичною освітою та досвідом у сфері біостатистики. Ці фахівці знають принципи і стандарти клінічних досліджень.
Як проходять дослідження
Дослідження проходять у декілька етапів, їх називають фазами.
1
I фаза. Вивчення того, чи є в ліків побічні ефекти. Для цього набирають здорових добровольців, які на кілька днів лягають у спеціальний медцентр – в Україні таких чотири – і за графіком приймають невелику дозу препарату. У медцентрі є реанімація, люди знаходяться під цілодобовим наглядом. Якщо в ліків є побічний ефект, то він проявляється зазвичай протягом 24–36 годин після приймання. Але із критичними випадками у «Фармаксі» не стикалися.
2
II фаза. Дослідження ефективності препарату на пацієнтах і пошук вірного дозування ліків. Для цього залучають пацієнтів із хворобою, з якою бореться препарат, і ділять їх на групи. Різним групам дають різні дозування і дивляться на реакцію організму. «Коли досліджують вакцини, щеплення роблять тільки здоровим людям, але різними дозами або кількістю введень, – розповідає експерт. – А потім дивляться, як часто хворіють вакциновані і невакциновані люди». На цьому етапі «Фармаксі» аналізує дані, які лікарі вносять в електронну систему управління клінічними дослідженнями OnlineCRF. Цю програму розробив IT-відділ «Фармаксі».
3
III фаза. Вивчення на великих групах пацієнтів, наскільки ефективними є ліки в порівнянні з відомим препаратом або плацебо. Пацієнтів розділяють на дві групи. Перша отримує нові ліки, друга – стандартне лікування. «Завдання цієї фази – перевірити ефективність на людях різної статі, віку, з різними супутніми хворобами, які приймають супутні ліки», – пояснює Юрій Лебідь.
На другому і третьому етапах тестування «Фармаксі» укладає договори з лікарями, з логістичними компаніями, які розвозять ліки по лікарнях, дотримуючись температурного режиму, зі складами, де зберігатимуться ліки. Якщо препарат везуть з-за кордону, компанія може взяти на себе розмитнення і сплату податків.
Чому результатам досліджень можна вірити
На всіх етапах клінічних випробувань, крім першого, ані лікар, ані пацієнт не знають, чи приймає людина досліджуваний препарат або вже схвалений. «Це подвійний сліпий метод дослідження: лікарям видають тільки пронумеровані коробки із препаратами. Пацієнтам теж не говорять, у яку групу вони потрапили», – підкреслює експерт.
Окремі фахівці «Фармаксі» – монітори – приїжджають у лікарні і звіряють інформацію, яку лікарі внесли в електронну систему OnlineCRF, з тим, що написано в історії хвороби.
Якщо лікарі щось не врахували або переплутали, монітори це відстежують і виправляють. Самі медики не можуть непомітно редагувати записи, – каже Юрій Лебідь.
Після кожної фази дослідження «Фармаксі» подає документи в Державний експертний центр, який повинен схвалити продовження випробувань. За кожну послугу компанія бере гроші у виробника ліків. Наприклад, скласти протокол дослідження коштує $3–5 тис., статистична обробка даних – $2–4 тис.
Коли три фази дослідження пройшли успішно і в Експертного центру немає зауважень, препарат реєструють. Тільки після цього він потрапляє в аптеки.
Інші країни можуть автоматично зареєструвати ті препарати, які вже пройшли реєстрацію в Європі або США. Якщо західний виробник проводить дослідження в 5–10 країнах, включаючи Україну, то він сам вибирає, у якій країні реєструвати препарат.
Але на цьому дослідження не закінчуються. Після реєстрації препарати проходять IV фазу випробувань. Вона потрібна, щоб зрозуміти, чи немає неврахованих побічних явищ. Якщо вони виявляться, лікарі або пацієнти повинні повідомити про це в Експертний центр, і ліки можуть зняти з реєстрації.
Як тестують вакцини
За словами Юрія Лебідя, клінічні дослідження одних ліків можуть тривати 3–5 років. Це залежить від того, скільки часу займає курс лікування, скільки пацієнтів беруть участь у тестуванні та інших факторів.
Для дослідження вакцин залучають більше людей, ніж для вивчення звичайних ліків, – приблизно 40 тис. осіб.

Юрій Лебідь, засновник «Фармаксі»
Тестуючи вакцину, перевіряють три фактори: зменшення смертності, кількості важких випадків і госпіталізацій вакцинованих людей у порівнянні з тими, хто не зробив щеплення.
Кожна країна може затверджувати свій рівень безпеки й ефективності вакцини, єдиного стандарту немає.
Як тестували вакцини від коронавірусу
Індійська CoviShield, китайська CoronaVac та інші вакцини проти COVID-19, які застосовують в Україні й інших країнах, теж проходять три фази досліджень. Різниця в тому, що через пандемію для реєстрації отримують мінімально необхідний, але досить переконливий результат. Регуляторні органи оцінюють ці результати досліджень і дають «екстрений» дозвіл на застосування вакцин. Це дозволяє швидше почати вакцинацію. Але завдання довести роботу до кінця і надати повні дані з виробника не знімають.
Безліч вакцин від відомих виробників не показали задовільні результати, і їх вивчення припинили. Міф про те, що фармкомпаніям вигідна епідемія, тому що вони заробляють на ній, далекий від дійсності. Чимало компаній вклали мільйони та мільярди доларів в розробку вакцини, але не змогли довести її ефективність і безпеку. У результаті вони зазнали величезних збитків.
Ось що відомо про дві вакцини, які довели ефективність і безпеку і їх зараз використовують в Україні.
1. Вакцина CoviShield – ліцензійний аналог шведсько-британської вакцини AstraZeneca.
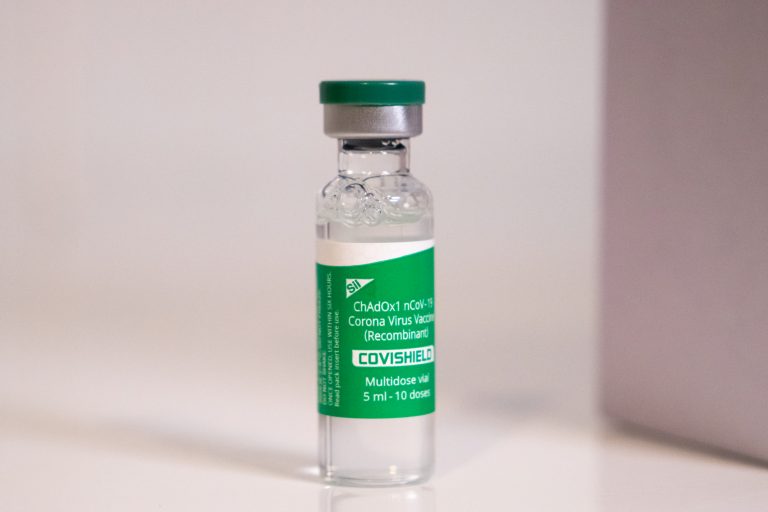
Фото з офіційного порталу Києва
Виробляють її в Інституті сироватки крові Індії. «Це векторна вакцина, – розповідає Юрій Лебідь. – Беруть частину РНК коронавірусу, поміщають в інший вірус, безпечний для людини аденовірус шимпанзе. Він стає вектором-переносником, який доставляє РНК коронавірусу в людський організм. У клітинах людини виробляється спеціальний вірусний білок (spike), організм у відповідь на це виробляє антитіла і тренує імунні клітини. Якщо коронавірус потрапить в організм вакцинованої людини, імунна система вже буде знати, як реагувати на вірусний білок, і тому буде ефективно боротися з вірусом».
III фазу клінічних досліджень AstraZeneca проводили в кілька етапів у Великій Британії, Бразилії і Південній Африці. У тестуванні взяли участь майже 24 тис. осіб віком від 18 і старші. Попередні результати показали ефективність 70,4%. Європейське агентство лікарських засобів (EMA) повідомляло про ефективніст 60%. Останні дані на сайті самої компанії AstraZeneca кажуть, що ефективність досягає вже 79%, а важкій формі хвороби вакцина запобігає на 100%.
Побічні реакції, які спостерігали під час дослідження першої дози – біль у місці уколу, головний біль, підвищена температура, втома, озноб, – проходили протягом декількох днів після вакцинації. Після другої дози вони зустрічалися рідше.
Вакцину CoviShield схвалили серед інших Канада й Угорщина. Індія направила в інші країни більше ніж 60 млн доз вакцини.
2. Вакцину CoronaVac виробляє китайська компанія Sinovac Biotech.
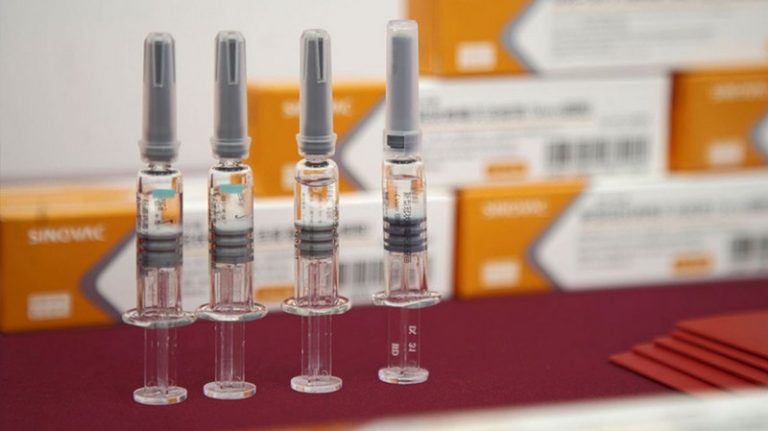
Фото з порталу Вінницької ОДА
Це інактивована вакцина, у її основі – неживі частинки вірусу. Заразити людину такою вакциною не можна, але антитіла проти вірусу організм виробляє. «Це традиційний метод отримання вакцин», – розповідає Юрій Лебідь.
Як і шведсько-британська, китайська вакцина показала різну ефективність на різних етапах III фази досліджень: у Туреччині – 91%, а в Бразилії, де добровольцями стали більше ніж 12 тисяч лікарів, – трохи вище 50%. Серед побічних ефектів – біль і почервоніння в місці уколу, підвищена температура.
Крім України вакцину схвалили в Китаї, Азербайджані, Бразилії, Чилі, Індонезії та Туреччині.
Компанія «Фармаксі» розробляла програму клінічного дослідження цієї вакцини, але проєкт в Україні не запустився. Зараз «Фармаксі» тестує ліки від COVID-19.
Що дослідження дають Україні
За вісім років «Фармаксі» досліджувала в Україні препарати, які випускають фармкомпанії із США, Канади, Франції, Південної Кореї та інших країн.
«До нас звертаються, тому що дослідження в Україні проводяться на високому рівні, їх схвалюють європейські та північноамериканські регуляторні органи. До того ж Україна – велика країна, де можна знайти потрібну кількість пацієнтів з різними захворюваннями», – пояснює Юрій Лебідь.
За участь в I фазі досліджень пацієнтам платять від 10 до 20 тис. грн. За участь у II і III фазах пацієнтові не платять, зате він безкоштовно отримує лікування, іноді дуже дороге. Якщо досліджується препарат від лейкозу, вартість курсу може досягати 2,5 млн грн, а таких курсів потрібно два-три на рік. Для людей, які вже продали все, участь у дослідженні може стати останнім шансом зберегти життя.
«Пацієнти отримують терапію майбутнього. Їм видають супутні препарати, наприклад, жарознижувальне при випробуванні ліків від коронавірусу, іноді оплачують таксі до лікарні та додому», – додає Юрій Лебідь.
Лікарі теж отримують гонорар за участь у дослідженнях – від $500 до $3 тис. за пацієнта в залежності від складності проєкту. Таким чином у країні, де проводять тестування, залишаються десятки, а то і сотні тисяч доларів.
Попри очевидну вигоду для пацієнтів та економіки, в Україні проводиться мало досліджень. «У США проходять 12–15 тис. досліджень на рік, у Німеччині та Польщі – приблизно 3 тис., а в нас – у середньому 300», – наводить цифри співзасновник «Фармаксі».
Чому в Україні погано розвивається ринок клінічних досліджень
За словами Юрія Лебідя, у цього є кілька причин.
- У країні мало інноваційних фармацевтичних розробок. «Олександра Кужель якось заявила, що зарубіжні фармкомпанії ставлять досліди на українцях, це розтиражували ЗМІ, – наводить приклад Юрій Лебідь. – Але у фармкомпаній інша логіка. Вони вкладають багато грошей у розробку препарату, щоб він успішно показав себе під час досліджень. Допомагав від хвороби, від якої більше нічого не допомагає. Чим кращий препарат, тим більше продажів».
- В Україні тільки три великі фармацевтичні компанії займаються інноваційними розробками. Але українські пацієнти, яким пропонують участь у дослідженнях, начитавшись сумнівних статей, бачать у всьому підступ. «Лікарі розповідають: “Люди погоджуються на участь у програмі, приходять додому, а родичі їм кажуть, що вони божевільні, це отрута”, – цитує експерт. – Уранці ці пацієнти телефонують лікареві і відмовляються. Якщо це хворі на рак – вони буквально йдуть вмирати».
Ще один наочний приклад – ставлення до вакцин.
«Коли більше половини населення не хоче вакцинуватися – це катастрофа», – вважає Юрій Лебідь. Українці відкидають усі досягнення науки, а влада провалює інформаційну кампанію з вакцинації.
Команда «Фармаксі» за вісім років вивчила приблизно сорок ліків. «Тільки двоє з них виявилися неефективними і не пройшли III фазу тестування. Перші від діабету, другі від ревматоїдного артриту. При цьому вони були досить безпечними», – підкреслює Юрій Лебідь.
Під час досліджень у людей бувають побічні ефекти. Але вони виникають не набагато частіше, ніж при лікуванні вже зареєстрованими препаратами. «Було дослідження, у якому порівнювали частоту побічних ефектів при звичайному лікуванні і під час досліджень. Виявилося, що вони приблизно однакові», – розповідає співзасновник «Фармаксі».
Ще один міф – що українці беруть участь у дослідженнях без свого відома. Насправді, кожен учасник підписує інформовану згоду. Перед цим лікар розповідає йому про ризики та переваги участі в дослідженні. «Це сувора вимога, яку жорстко контролюють», – підкреслює Юрій Лебідь.
- Бюрократія. Вона призводить до того, що навіть українські фармкомпанії часто проводять дослідження в інших країнах: Чехії, Йорданії. «Щоб отримати дозвіл Експертного центру МОЗ на старт дослідження, потрібно чекати два місяці. А в Польщі або Чехії – два тижні. Схвалення перед II і III фазами в нас видають за чотири-п’ять місяців, а в інших країнах – за три», – перераховує експерт.
На його думку, якщо нічого не зміниться, з України можуть піти і ті клієнти, які вже проводили в нас дослідження. А багато хворих втратять шанс отримати дороге лікування, забути про тяжкі хвороби або поліпшити своє здоров’я.













Повідомити про помилку
Текст, який буде надіслано нашим редакторам: